SOMAVERT 20 mg por és oldószer oldatos injekcióhoz
Hatóanyag:
pegvisomant
Csak vényre kapható
Kiszerelés:
30x

Tájékoztató ár:
-
Normatív TB-támogatás:
Nem
Eü. emelt támogatás:
Nem
-
Gyógyszerfőkategória:
HYPOPHYSIS ELÜLSŐ LEBENY HORMONOK
-
Törzskönyvi szám:
EU/1/02/240/003
-
Gyógyszeralkategória:
Az elülső hypophysis egyéb hormonjai és analógjaik
-
Gyártó:
Pfizer Europe
Betegtájékoztató
1. Milyen típusú gyógyszer a SOMAVERT és milyen betegségek esetén alkalmazható?
A SOMAVERT-et akromegália kezelésére alkalmazzák, amely a növekedési hormon és az IGF-I (inzulin-szerű növekedési faktor) fokozott termelődésével járó, a csontok túltengésével, lágyrészek duzzanatával, szívbetegséggel és ezekhez kapcsolódó betegségekkel jellemezhető hormonbetegség.
A SOMAVERT hatóanyaga, a pegviszomant, a növekedési hormon receptorát gátló anyag. Ezek az anyagok csökkentik a növekedési hormon hatását, valamint a vérben keringő IGF-I (inzulin-szerű növekedési faktor) szintjét.
2. Tudnivalók a SOMAVERT alkalmazása előtt
Ne alkalmazza a SOMAVERT-et
- ha allergiás a pegviszomantra vagy a gyógyszer (6. pontban felsorolt) egyéb összetevőjére.
Figyelmeztetések és óvintézkedések
A SOMAVERT alkalmazása előtt beszéljen kezelőorvosával, gyógyszerészével vagy a gondozását végző egészségügyi szakemberrel.
- Ha látászavart vagy fejfájást tapasztal, azonnal forduljon kezelőorvosához.
- Orvosa nyomon fogja követni a vérében keringő IGF-1 (inzulin-szerű növekedési faktor) szintjét és szükség szerint módosítja a SOMAVERT adagját.
- Kezelőorvosa ellenőrzi az adenómát (jóindulatú daganat) is.
- Kezelőorvosa megvizsgálja a májműködését a SOMAVERT-tel történő kezelés megkezdése előtt, illetve a kezelés alatt. Ha a vizsgálat kóros eredményekkel jár, kezelőorvosa megbeszéli Önnel a kezelési lehetőségeket. A kezelés megkezdésekor kezelőorvosa a SOMAVERT-tel történő kezelés első 6 hónapja során 4-6 hetente ellenőrzi vére májenzimszintjét. A SOMAVERT alkalmazását abba kell hagyni, ha májbetegség panaszai állnak fenn.
- Ha Ön cukorbeteg, előfordulhat, hogy kezelőorvosának meg kell változtatnia az Ön által alkalmazott inzulin vagy egyéb gyógyszerek adagját.
- Nőbetegeknél a fogamzóképesség megnövekedhet a betegség javulásával párhuzamosan. Ezt a gyógyszert nem javasolt terhes nőknél alkalmazni, a fogamzóképes nőknek pedig fogamzásgátlás alkalmazását kell tanácsolni (lásd még a terhességről szóló fejezetet alább).
Egyéb gyógyszerek és a SOMAVERT
Feltétlenül tájékoztassa kezelőorvosát, ha egyidejűleg egyéb gyógyszert alkalmaz akromegália vagy a cukorbetegség kezelésére.
Feltétlenül tájékoztassa kezelőorvosát vagy gyógyszerészét a jelenleg vagy nemrégiben alkalmazott, valamint alkalmazni tervezett egyéb gyógyszereiről.
A kezelés részeként egyéb gyógyszereket is kaphat. Fontos, hogy a SOMAVERT mellett minden gyógyszerét továbbra is alkalmazza, mindaddig, amíg kezelőorvosa, gyógyszerésze vagy a gondozását végző egészségügyi szakember másképpen nem utasítja.
Terhesség, szoptatás és termékenység
Terhes nőknek a SOMAVERT alkalmazása nem ajánlott. Amennyiben Ön fogamzóképes nő, a kezelés során fogamzásgátlást kell alkalmaznia.
Nem ismert, hogy a pegviszomant átjut-e az anyatejbe. A SOMAVERT-kezelés alatt nem szoptathat, hacsak meg nem beszélte ezt kezelőorvosával.
Ha Ön terhes vagy szoptat, illetve ha fennáll Önnél a terhesség lehetősége vagy gyermeket szeretne, a gyógyszer alkalmazása előtt beszéljen kezelőorvosával vagy gyógyszerészével.
A készítmény hatásai a gépjárművezetéshez és a gépek kezeléséhez szükséges képességekre
Nem végeztek vizsgálatokat a gépjárművezetéshez és gépek kezeléséhez szükséges képességekre gyakorolt hatással kapcsolatban.
A SOMAVERT nátriumot tartalmaz
Ez a gyógyszer kevesebb, mint 1 mmol (23 mg) nátriumot tartalmaz adagonként, azaz gyakorlatilag "nátriummentes".
3. Hogyan kell alkalmazni a SOMAVERT-et?
A gyógyszert mindig a kezelőorvosa vagy gyógyszerésze által elmondottaknak megfelelően alkalmazza. Amennyiben nem biztos az adagolást illetően, kérdezze meg kezelőorvosát vagy gyógyszerészét.
Kezdésként kezelőorvosa 80 mg pegviszomantot fog Önnek beadni szubkután (a bőr alá). Ezt követően a pegviszomant szokásos napi adagja 10 mg, amelyet szubkután (bőr alá adott) injekció formájában kap.
Négy-hat hetente a vér úgynevezett IGF-I-szintje alapján, a megfelelő terápiás hatás elérése céljából, kezelőorvosa módosítani fogja az adagot, a pegviszomant napi 5 mg-onkénti emelésével.
Az alkalmazással kapcsolatos tudnivalók:
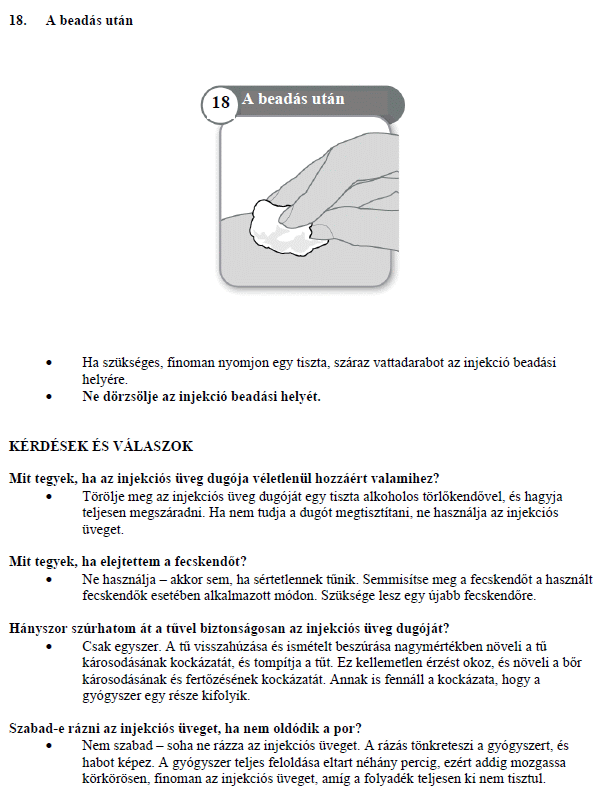
A SOMAVERT-et a bőr alá kell beadni. Az injekciót saját maga vagy egy másik személy, pl. kezelőorvosa vagy asszisztense adhatja be. Feltétlenül kövesse az e tájékoztató végén található, az injekció beadásáról szóló részletes leírás utasításait. A gyógyszer alkalmazását mindaddig folytassa, amíg kezelőorvosa Önt erre utasítja.
Ezt a gyógyszert beadás előtt fel kell oldani. Az injekciót tilos más gyógyszert tartalmazó fecskendőben vagy injekciós üvegben összekeverni.
Az injekció helyén a bőr alatti zsírszövet megvastagodhat. Ennek elkerülése érdekében, minden egyes injekciózás alkalmával más helyet válasszon az injekció beadására, a betegtájékoztató "2. LÉPÉS: AZ INJEKCIÓ BEADÁSA" című fejezetében leírtak szerint. Ez időt ad bőrének és a bőr alatti területeknek, hogy visszanyerje állapotát, mielőtt a következő injekció beadása ugyanarra a helyre történne.
Ha Ön úgy érzi, hogy a gyógyszer hatása túl erős vagy túl gyenge, forduljon kezelőorvosához, gyógyszerészéhez vagy a gondozását végző egészségügyi szakemberhez.
Ha az előírtnál több SOMAVERT-et alkalmazott
Ha Ön véletlenül több SOMAVERT-et adott be, mint amennyit kezelőorvosa előírt, nem valószínű, hogy ez súlyos következményekkel járna, de azonnal forduljon kezelőorvosához, gyógyszerészéhez vagy a gondozását végző egészségügyi szakemberhez.
Ha elfelejtette alkalmazni a SOMAVERT-et
Ha elfelejti beadni az egyik injekciót, adja be magának a következő adagot, amikor eszébe jut, és folytassa a SOMAVERT adagolását úgy, ahogy kezelőorvosa előírta. Ne alkalmazzon dupla adagot az elfelejtett adag pótlására.
Ha bármilyen további kérdése van a gyógyszer alkalmazásával kapcsolatban, kérdezze meg kezelőorvosát, gyógyszerészét vagy a gondozását végző egészségügyi szakembert.
4. Lehetséges mellékhatások
Mint minden gyógyszer, így ez a gyógyszer is okozhat mellékhatásokat, amelyek azonban nem mindenkinél jelentkeznek.
Az enyhétől a súlyosig terjedő allergiás reakciókat jelentettek néhány SOMAVERT-et alkalmazó betegnél. A súlyos allergiás reakció tünetei közé tartozhat a következők közül egy vagy több: az arc, a nyelv, az ajkak vagy a torok duzzanata; zihálás vagy nehézlégzés (a gége izmainak görcsös összehúzódása); az egész testre kiterjedő bőrkiütés, csalánkiütés (urtikária) vagy viszketés; vagy szédülés. Azonnal értesítse kezelőorvosát, ha bármelyik e tünetek közül kialakul.
Nagyon gyakori: 10 betegből több mint 1-et érinthet
- Fejfájás.
- Hasmenés.
- Ízületi fájdalom.
Gyakori: 10 betegből legfeljebb 1-et érinthet
- Légszomj.
- A máj működését jelző anyagok szintjének emelkedése. Ezek a vérkép eredményeiben láthatók.
- Vér a vizeletben.
- Vérnyomás-emelkedés.
- Székrekedés, hányinger, hányás, puffadásérzés, emésztési zavar, gázok.
- Szédülés, álmosság, nem befolyásolható remegés, csökkent tapintásérzés.
- Véraláfutás vagy vérzés az injekció beadási helyén, fájdalom vagy duzzanat az injekció beadási helyén, a bőralatti zsírszövet megvastagodása az injekció beadási helyén, végtagok duzzanata, gyengeség, láz.
- Izzadás, viszketés, kiütés, véraláfutásra való hajlam.
- Izomfájdalom, ízületi gyulladás.
- A vér koleszterinszintjének megemelkedése, hízás, vércukorszint-emelkedés, vércukorszint- csökkenés.
- Influenzaszerű betegség, fáradtság.
- Szokatlan álmok.
- Szemfájdalom.
Nem gyakori: 100 betegből legfeljebb 1-et érinthet
- Allergiás reakció a beadást követően (láz, bőrkiütés, viszketés és súlyos esetben légzési nehézség, a bőr gyors megduzzadása, amely sürgős orvosi figyelmet igényel). Bekövetkezhet azonnal, vagy néhány nappal a beadás után is.
- Fehérje a vizeletben, vizelet mennyiségének megnövekedése, veseproblémák.
- Érdeklődés hiánya, zavartságérzés, fokozott szexuális vágy, pánikroham, feledékenység, alvásproblémák.
- Vérlemezkék számának csökkenése a vérben, megnövekedett vagy csökkent fehérvérsejtszám a vérben, vérzésre való hajlam.
- Szokatlan érzés, csökkent sebgyógyulási hajlam.
- A szem túlerőltetése, belsőfülproblémák.
- Arc duzzanata, száraz bőr, éjszakai izzadás, a bőr kipirosodása (eritéma), viszkető kiemelkedések a bőrön (csalánkiütés).
- A zsírok mennyiségének növekedése a vérben, étvágy megnövekedése.
- Szájszárazság, fokozott nyálelválasztás, fogproblémák, aranyér.
- Rendellenes ízérzés, migrén.
Nem ismert: a rendelkezésre álló adatokból nem állapítható meg
- Düh.
- Súlyos légszomj (gégegörcs).
- A bőr és a bőr alatti szövetek, valamint a szöveteket bélelő réteg (nyálkahártya) gyors megduzzadása (angioödéma).
A kezelés során a betegek kb. 17%-ánál ellenanyag termelődik a növekedési hormonnal szemben. Az ellenanyagok nem gátolják ennek a gyógyszernek a hatását.
Mellékhatások bejelentése
Ha Önnél bármilyen mellékhatás jelentkezik, tájékoztassa kezelőorvosát, gyógyszerészét vagy a gondozását végző egészségügyi szakembert. Ez a betegtájékoztatóban fel nem sorolt bármilyen lehetséges mellékhatásra is vonatkozik. A mellékhatásokat közvetlenül a hatóság részére is bejelentheti a https://mellekhatas.ogyei.gov.hu/ weboldalon.
A mellékhatások bejelentésével Ön is hozzájárulhat ahhoz, hogy minél több információ álljon rendelkezésre a gyógyszer biztonságos alkalmazásával kapcsolatban.
5. Hogyan kell a SOMAVERT-et tárolni?
A gyógyszer gyermekektől elzárva tartandó!
A címkén és a dobozon feltüntetett lejárati idő (Felhasználható) után ne alkalmazza ezt a gyógyszert. A lejárati idő az adott hónap utolsó napjára vonatkozik.
A port tartalmazó injekciós üveg(ek) hűtőszekrényben (2 °C - 8 °C) tárolandó(k). A fénytől való védelem érdekében a port tartalmazó injekciós üveg(ek)et tartsa a dobozában/dobozaikban. Nem fagyasztható!
A SOMAVERT por injekciós üvegét/üvegeit tartalmazó doboz(ok) egy egyszeri, legfeljebb 30 napos időszakig tárolható(k) szobahőmérsékleten (legfeljebb 25 °C-on). A szavatossági időt (év/hónap/nap) fel kell tüntetni a dobozon (a hűtőszekrényből történő kivétel időpontjától számítva legfeljebb 30 nap). Az injekciós üvege(ke)t óvni kell a fénytől. Ne tegye vissza a gyógyszert a hűtőszekrénybe.
Ha nem használják fel az új szavatossági időpontig vagy a dobozon szereplő lejárati időig (azt az időpontot kell figyelembe venni, amelyikre hamarabb kerül sor), a gyógyszert meg kell semmisíteni. Az előretöltött fecskendő(k) legfeljebb 30 °C-on tárolandó(k), illetve tárolható(k) hűtőszekrényben (2 °C - 8 °C) is. Nem fagyasztható!
A SOMAVERT oldat elkészítése után a készítményt azonnal fel kell használni.
Ne alkalmazza a gyógyszert, ha az oldat zavaros vagy szemcséket tartalmaz.
Semmilyen gyógyszert ne dobjon a szennyvízbe vagy a háztartási hulladékba. Kérdezze meg gyógyszerészét, hogy mit tegyen a már nem használt gyógyszereivel. Ezek az intézkedések elősegítik a környezet védelmét.
6. A csomagolás tartalma és egyéb információk
Mit tartalmaz a SOMAVERT?
- A készítmény hatóanyaga a pegviszomant.
- SOMAVERT 10 mg: 10 mg pegviszomant por injekciós üvegenként. 1 ml oldattal történő feloldás után 1 ml oldat 10 mg pegviszomantot tartalmaz.
- SOMAVERT 15 mg: 15 mg pegviszomant por injekciós üvegenként. 1 ml oldattal történő feloldás után 1 ml oldat 15 mg pegviszomantot tartalmaz.
- SOMAVERT 20 mg: 20 mg pegviszomant por injekciós üvegenként. 1 ml oldattal történő feloldás után 1 ml oldat 20 mg pegviszomantot tartalmaz.
- SOMAVERT 25 mg: 25 mg pegviszomant por injekciós üvegenként. 1 ml oldattal történő feloldás után 1 ml oldat 25 mg pegviszomantot tartalmaz.
- SOMAVERT 30 mg: 30 mg pegviszomant por injekciós üvegenként. 1 ml oldattal történő feloldás után 1 ml oldat 30 mg pegviszomantot tartalmaz.
- Egyéb összetevők: glicin, mannit (E421), vízmentes dinátrium-hidrogén-foszfát,
nátrium-dihidrogén-foszfát-monohidrát (lásd 2. pont "A SOMAVERT nátriumot tartalmaz").
- Az oldószer injekcióhoz való víz.
Milyen a SOMAVERT külleme és mit tartalmaz a csomagolás?
A SOMAVERT injekcióhoz való por és oldószer formájában kapható (10 mg, 15 mg, 20 mg, 25 mg vagy 30 mg pegviszomant injekciós üvegben és 1 ml oldószer előretöltött fecskendőben). 1 darabos vagy 30 darabos kiszerelés. Nem feltétlenül mindegyik kiszerelés kerül kereskedelmi forgalomba. Fehér por és tiszta, színtelen oldat.
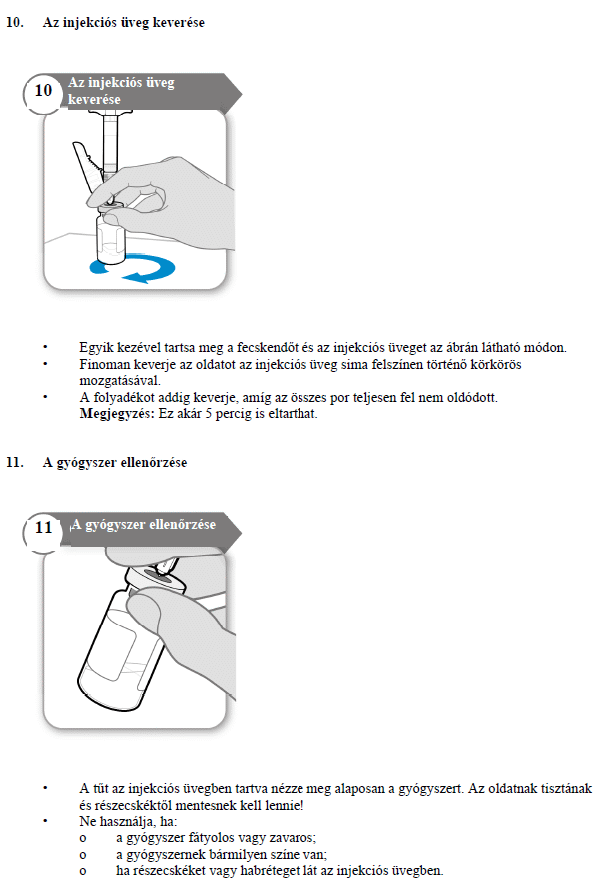
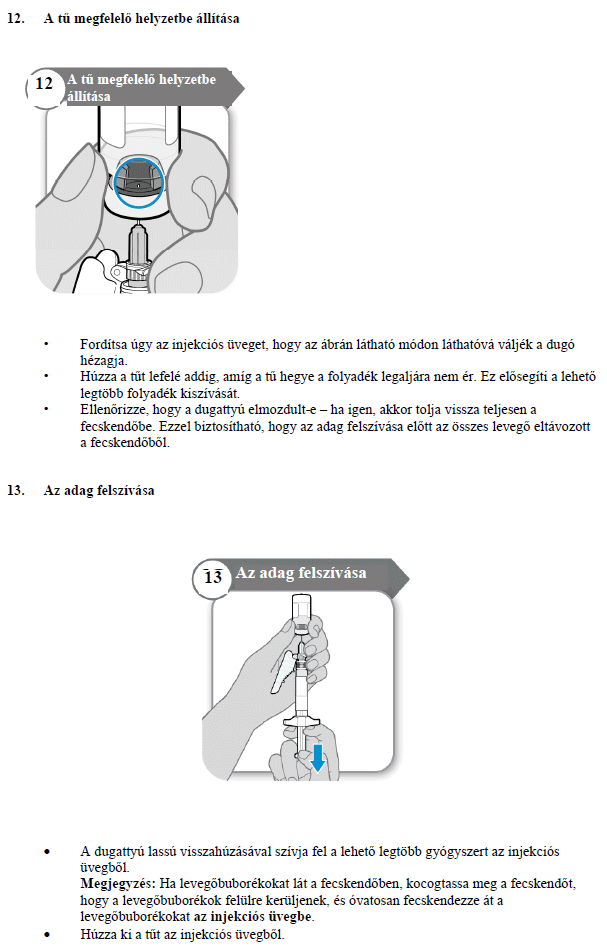
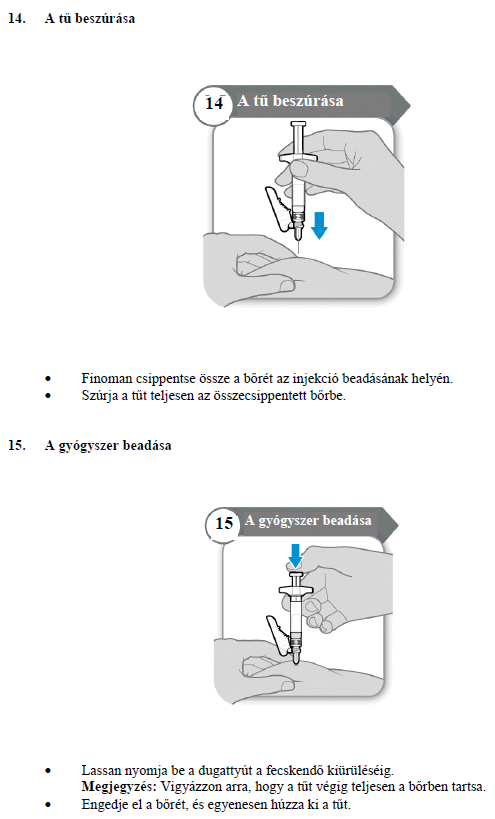
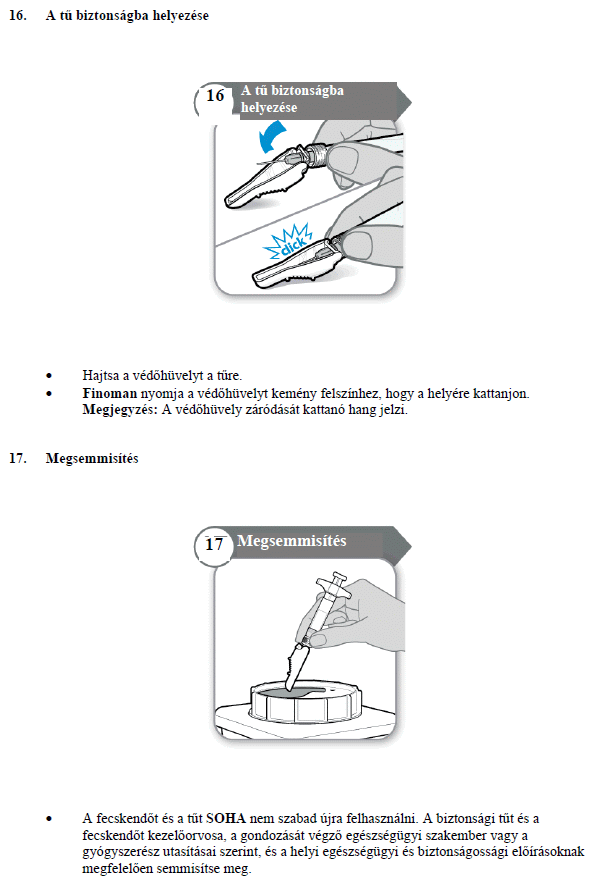
HASZNÁLATI UTASÍTÁS
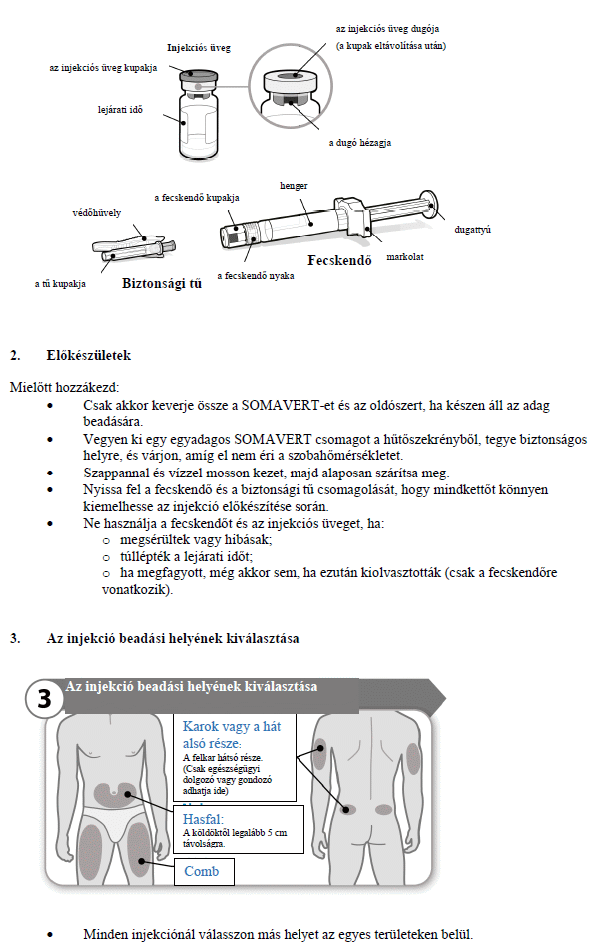
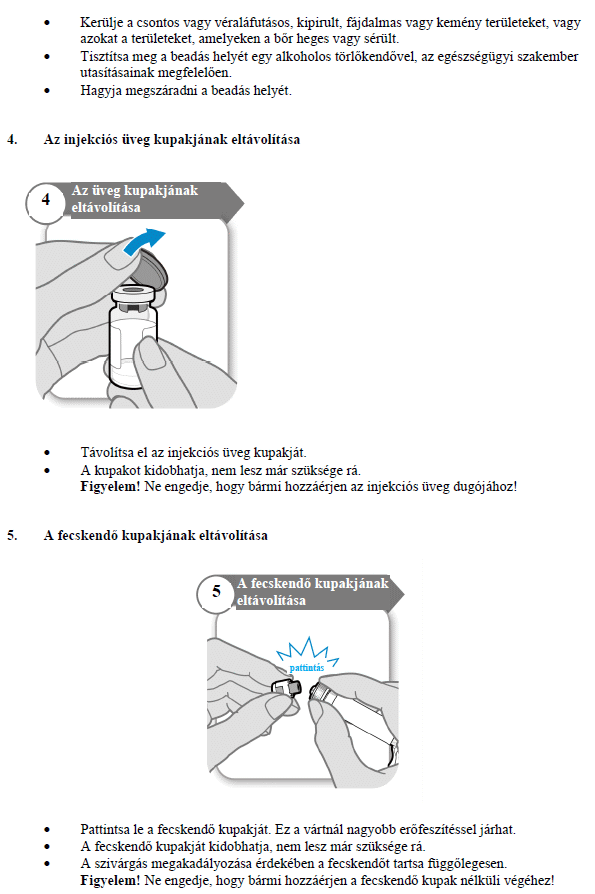
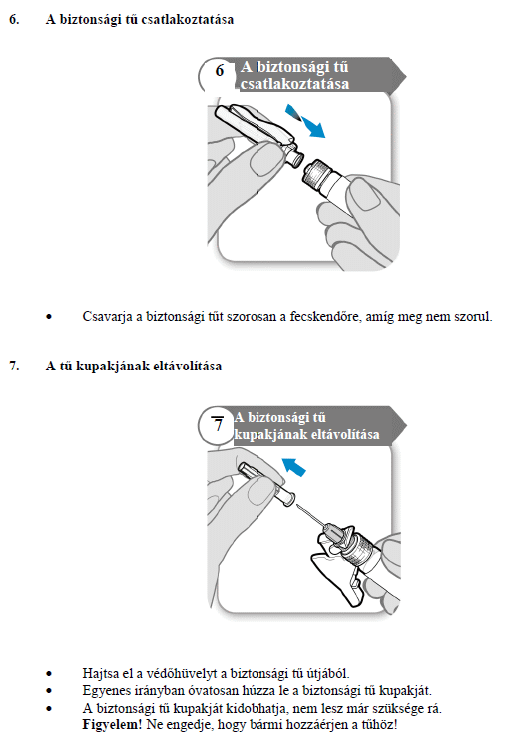
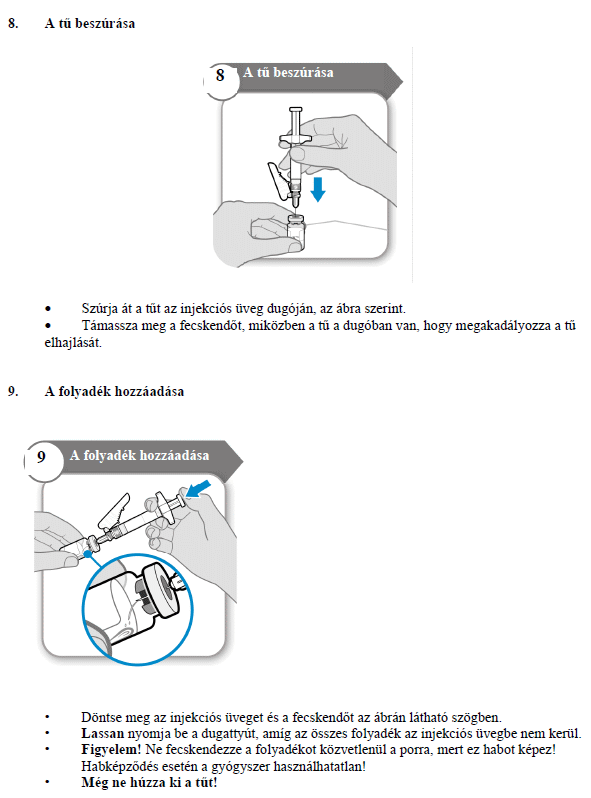
A szöveg publikálásának dátuma az ema.europa.eu weboldalon: 2023.11.27.
