RUCONEST 2100 egység por és oldószer oldatos injekcióhoz
Hatóanyag:
conestat alfa
Csak vényre kapható
Kiszerelés:
1x

Tájékoztató ár:
-
Normatív TB-támogatás:
Nem
Eü. emelt támogatás:
Nem
-
Gyógyszerfőkategória:
EGYÉB HAEMATOLOGIAI ANYAGOK
-
Törzskönyvi szám:
EU/1/10/641/002
-
Gyógyszeralkategória:
Örökletes angiooedema gyógyszerei
-
Gyártó:
Pharming Group
Betegtájékoztató
1. Milyen típusú gyógyszer a Ruconest és milyen típusú betegségek esetén alkalmazható?
A Ruconest hatóanyaga az alfa-konesztát. Az alfa-konesztát a humán C1 inhibitor rekombináns (nem vérkészítmény) formája (rhC1-INH).
A Ruconest alkalmazása egy ritka, örökletes angioödéma (HAE) néven ismert, öröklött vérképzőszervi betegségben javallott, felnőttek, serdülők és (2 éves vagy annál idősebb) gyermekek számára. Az ilyen betegek vérében kevés a C1 gátló fehérje, aminek következtében ismételt rohamok formájában duzzanat, hasi fájdalom, nehézlégzés és egyéb tünetek fordulhatnak elő.
A Ruconest alkalmazásának célja a C1 gátló hiány mérséklése, ami által az akut HAE-roham során mérséklődnek a tünetek.
2. Tudnivalók a Ruconest alkalmazása előtt
Ne alkalmazza a Ruconest-et:
- ha allergiás, vagy megítélése szerint allergiás a nyulakra.
- ha allergiás az alfa-konesztátra vagy a gyógyszer (6. pontban felsorolt) egyéb összetevőjére.
Figyelmeztetések és óvintézkedések
A Ruconest alkalmazása előtt beszéljen kezelőorvosával.
Ha a Ruconest beadása után allergiás reakciókat, pl. csalánkiütést, bőrkiütést (rash), viszketést, szédülést, zihálást, nehézlégzést tapasztal, vagy feldagad a nyelve, kérjen sürgősségi orvosi ellátást, hogy az allergiás reakció tünetei sürgősen kezelhetőek legyenek.
Fontos, hogy a Ruconest alkalmazásának megkezdése előtt tájékoztassa kezelőorvosát arról, ha a véralvadást érintő probléma (trombózisos esemény) áll fenn Önnél, vagy ilyen probléma korábban felmerült Önnél. Ebben az esetben szorosan megfigyelik az Ön állapotát.
A túlérzékenységi reakciók nem zárhatók ki; ezek tünetei hasonlíthatnak az angioödémás rohamokhoz.
Gyermekek és serdülők
A Ruconest alkalmazása nem javallt 2 évesnél fiatalabb gyermekek számára. A Ruconest alkalmazását 5 évesnél fiatalabb gyermekeknél nem vizsgálták. A kezelőorvos fogja eldönteni, hogy az Ön gyermeke kezelhető-e Ruconest-tel. A készítmény alkalmazása alatt és azt követően gyermekét fokozottan figyelni kell, hogy nem jelentkeznek-e nála az allergiás reakció tünetei.
Egyéb gyógyszerek és a Ruconest
Feltétlenül tájékoztassa kezelőorvosát a jelenleg vagy nemrégiben szedett, valamint szedni tervezett egyéb gyógyszereiről.
Amennyiben szöveti típusú plazminogén aktivátort kap akut vérrögoldó kezelésként, egyidejűleg nem részesülhet Ruconest-kezelésben.
Terhesség és szoptatás
A Ruconest alkalmazása terhesség vagy szoptatás idején nem ajánlott.
Ha gyermekvállalást tervez, erről a Ruconest alkalmazásának megkezdése előtt tájékoztassa kezelőorvosát.
A készítmény hatásai a gépjárművezetéshez és a gépek kezeléséhez szükséges képességekre
Ne vezessen gépjárművet, illetve ne kezeljen gépeket, ha a Ruconest alkalmazása után szédül vagy fejfájása van.
A Ruconest nátriumot tartalmaz (19,5 mg injekciós üvegenként)
Ezt kontrollált nátrium diéta esetén figyelembe kell venni.
3. Hogyan kell alkalmazni a Ruconest-et?
A Ruconest kezelést örökletes angioödéma megállapításában és kezelésében jártas szakorvos fogja kezdeményezni.
A Ruconest-et lassan, körülbelül 5 perc alatt, közvetlenül vénába kell beadnia egy egészségügyi szakembernek mindaddig, amíg Ön, vagy a gondozója megfelelő betanításban részesül és képessé válik a Ruconest alkalmazására.
Ezt a gyógyszert mindig pontosan a betegtájékoztatóban leírtaknak, vagy az Ön kezelőorvosa vagy a gondozását végző egészségügyi szakember által elmondottaknak megfelelően alkalmazza. Amennyiben nem biztos az adagolást illetően, kérdezze meg kezelőorvosát vagy a gondozását végző egészségügyi szakemberét.
A Ruconest-et vénába kell beadni körülbelül 5 perc alatt. Az alkalmazandó adagot az Ön testsúlya alapján határozzák meg.
Legtöbbször egyetlen adag elegendő. Egy további adag beadása is szükséges lehet, ha a tünetek felnőtteknél és serdülőknél 120 percen belül vagy gyermekeknél 60 percen belül nem javulnak.24 órán belül a 7. lépésnek megfelelően számítottak szerint legfeljebb 2 adag adható be.
Ön vagy gondozója a Ruconest-et csak azt követően fecskendezheti be, ha megfelelő utasításokat kapott, és betanításban részesült a kezelőorvosától vagy a gondozását végző egészségügyi szakembertől.
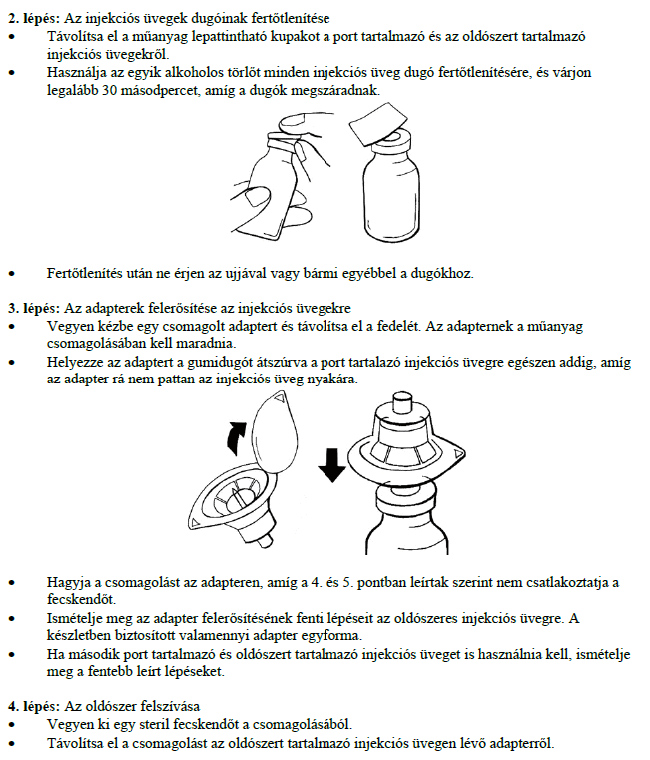
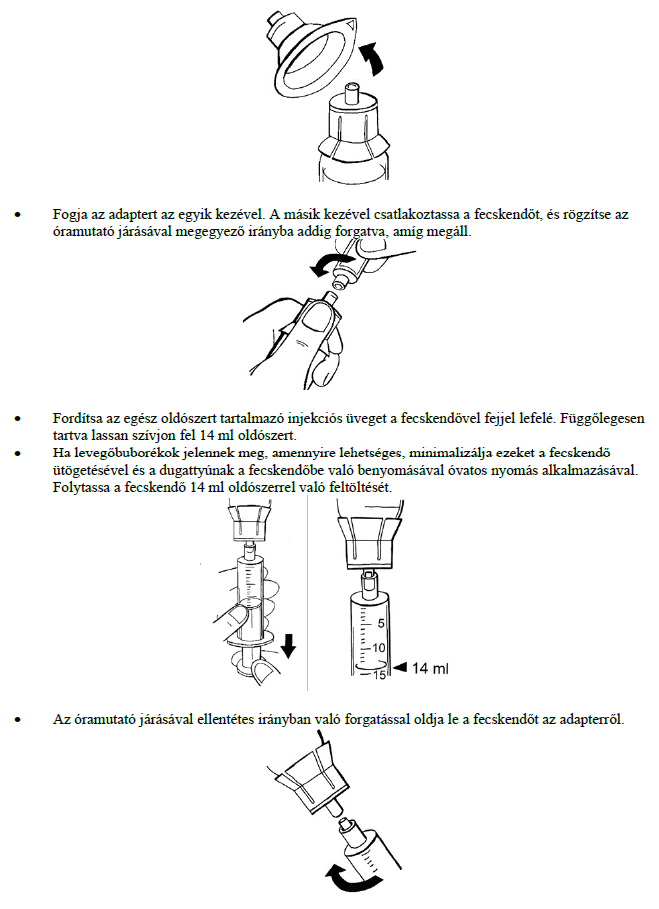
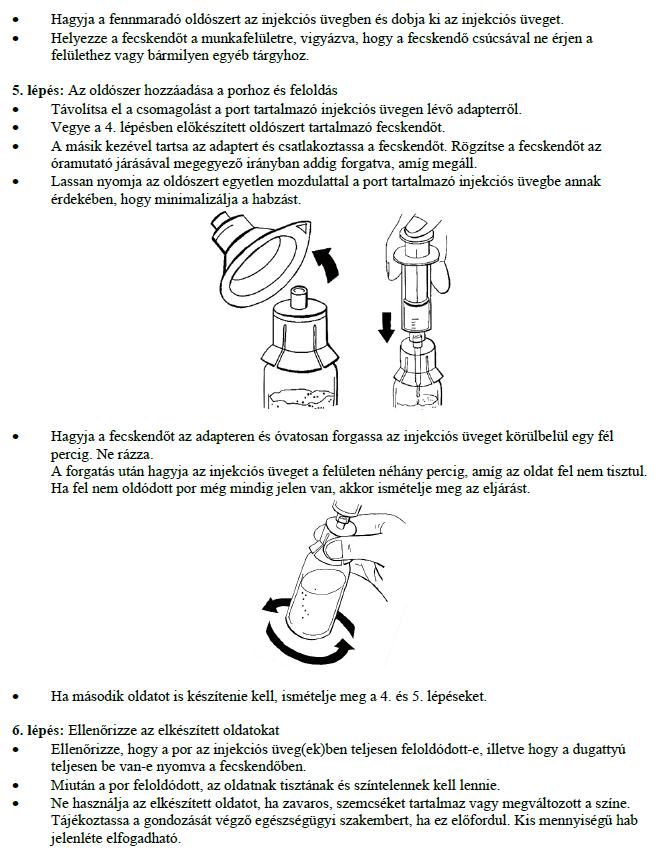
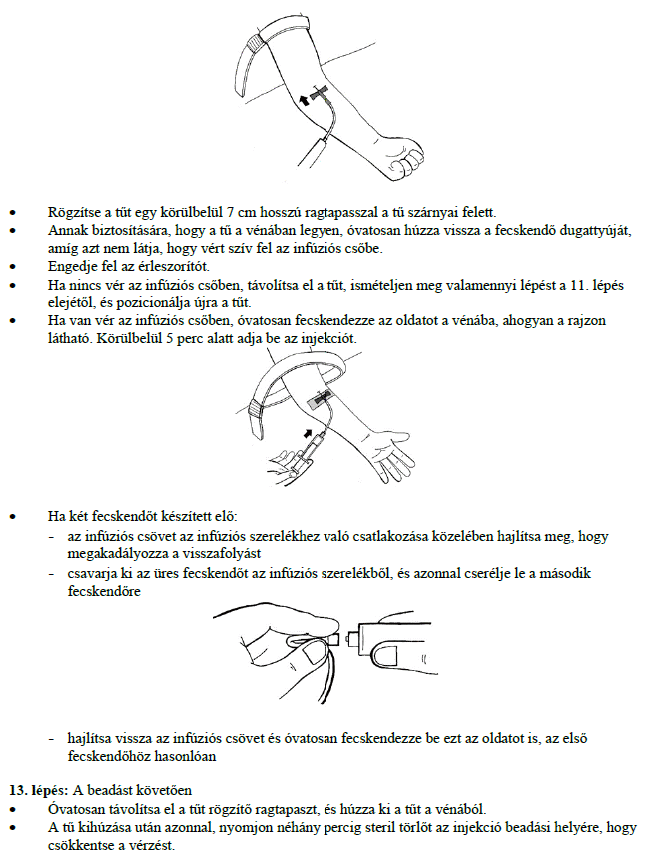
Használati utasítás
Ne keverje vagy alkalmazza a Ruconest-et más gyógyszerekkel vagy oldatokkal. Alább található annak leírása, hogy hogyan kell a Ruconest oldatot elkészíteni és alkalmazni.


Ha az előírtnál több Ruconest-et alkalmazott
Ha ez előfordul, lépjen kapcsolatba a kezelőorvosával vagy a legközelebbi kórházzal.
Ha bármilyen további kérdése van a gyógyszer alkalmazásával kapcsolatban, kérdezze meg kezelőorvosát.
4. Lehetséges mellékhatások
Mint minden gyógyszer, így ez a gyógyszer is okozhat mellékhatásokat, amelyek azonban nem mindenkinél jelentkeznek.
Amennyiben az Ön tünetei súlyosabbá válnak, és/vagy kiütések jelennek meg a bőrén, bizsergést, nehézlégzést tapasztal, vagy feldagad az arca vagy a nyelve, azonnal forduljon orvoshoz. Ez azt jelezheti, hogy allergiássá vált a Ruconest-re.
A Ruconest-kezelés idején előfordulhat néhány mellékhatás:
Gyakori (10 betegből legfeljebb 1 beteget érint):
- Hányinger
Nem gyakori (100 betegből legfeljebb 1 beteget érint):
- Hasi fájdalom, hasmenés
- Bizsergő, szúró érzés vagy zsibbadás a szájban.
- Fejfájás, szédülés
- A bőr vagy a végtagok tapintási érzékelésének csökkenése.
- Torokirritáció
- Csalánkiütés
- A fül és a fül körüli terület feldagadása
- Allergiás sokk
Nem ismert: a gyakoriság a rendelkezésre álló adatok alapján nem becsülhető meg
- Túlérzékenységi reakciók
Mellékhatások bejelentése
Ha Önnél bármilyen mellékhatás jelentkezik, tájékoztassa kezelőorvosát. Ez a betegtájékoztatóban fel nem sorolt bármilyen lehetséges mellékhatásra is vonatkozik. A mellékhatásokat közvetlenül a hatóság részére is bejelentheti az alábbi elérhetőségek valamelyikén keresztül:
Nemzeti Népegészségügyi és Gyógyszerészeti Központ, Postafiók 450, H-1372 Budapest
honlap: www.ogyei.gov.hu
elektronikus bejelentő form: https://mellekhatas.ogyei.gov.A mellékhatások bejelentésével Ön is hozzájárulhat ahhoz, hogy minél több információ álljon rendelkezésre a gyógyszer biztonságos alkalmazásával kapcsolatban.
5. Hogyan kell a Ruconest-et tárolni?
A gyógyszer gyermekektől elzárva tartandó!
A kartondobozon és az injekciós üveg címkéjén feltüntetett lejárati idő (EXP) után ne alkalmazza ezt a gyógyszert. A lejárati idő az adott hónap utolsó napjára vonatkozik.
Legfeljebb 25 °C-on tárolandó.
A fénytől való védelem érdekében a port tartalmazó injekciós üveget tartsa az injekciós üveg kartondobozában.
A Ruconest beadása előtt a port kell feloldani a csomagban található oldószerben (lásd 3. pont).
Feloldás után a készítményt azonnal fel kell használni.
Ne alkalmazza ezt a gyógyszert, ha feloldás után részecskéket vagy elszíneződést észlel az oldatban. Kis mennyiségű hab jelenléte elfogadható.
6. A csomagolás tartalma és egyéb információk
Mit tartalmaz a Ruconest?
Port tartalmazó injekciós üveg:
- A készítmény hatóanyaga az alfa-konesztát. Port tartalmazó injekciós üvegenként 2100 egység alfa-konesztátot tartalmaz, amely feloldás után 2100 egység/14 ml-nek vagy 150 egység/ml koncentrációnak felel meg.
- Egyéb összetevők a szacharóz, a nátrium-citrát (E331) és a citromsav.
Oldószert tartalmazó injekciós üveg:
- Az oldószer injekcióhoz való vizet tartalamz.
Milyen a Ruconest külleme és mit tartalmaz a csomagolás?
A Ruconest oldatos injekcióhoz való fehér vagy törtfehér port tartalmaz injekciós üvegben, együtt egy, a por feloldásához való tiszta és színtelen oldószert tartalmazó injekciós üveggel. A por injekcióhoz való vízben történő feloldása után az oldat tiszta és színtelen.
A Ruconest egy, az elkészítéshez és beadáshoz szükséges készletet tartalmazó kartondobozban kerül forgalomba, ami a következőket tartalmazza:
- 1 db, 2100 egység port tartalmazó injekciós üveg
- 1 db, 20 ml oldószert tartalmazó injekciós üveg
- 2 injekciós üveg adapter
- 1 fecskendő
- 1 infúziós szerelék 35 cm infúziós csővel és 25G tűvel
- 2 alkoholos törlő
- 1 steril, nem szövött törlő
- 1 öntapadó ragtapasz
A szöveg publikálásának dátuma az ema.europa.eu weboldalon: 2023.08.07.
