MOUNJARO 5 mg/adag KwikPen oldatos injekció előretöltött injekciós tollban
Hatóanyag:
tirzepatide
Csak vényre kapható
Kiszerelés:
1x2,4ml

Tájékoztató ár:
-
Normatív TB-támogatás:
Nem
Eü. emelt támogatás:
Nem
-
Gyógyszerfőkategória:
VÉRCUKORSZINT-CSÖKKENTŐ GYÓGYSZEREK, KIVÉVE INSULINOK
-
Törzskönyvi szám:
EU/1/22/1685/051
-
Gyógyszeralkategória:
Egyéb vércukorszint-csökkentő gyógyszerek, kivéve insulinok
-
Gyártó:
Eli Lilly Nederland
Ez a gyógyszer fokozott felügyelet alatt áll, mely lehetővé teszi az új gyógyszerbiztonsági információk gyors azonosítását. Ehhez Ön is hozzájárulhat a tudomására jutó bármilyen mellékhatás bejelentésével. A mellékhatások jelentésének módjairól a 4. pont végén (Mellékhatások bejelentése) talál további tájékoztatást.
Betegtájékoztató
1. Milyen típusú gyógyszer a Mounjaro KwikPen és milyen betegségek esetén alkalmazható?
A Mounjaro a tirzepatid nevű hatóanyagot tartalmazza, ami a 2-es típusú cukorbetegségben szenvedő felnőttek kezelésére szolgál. A Mounjaro csak akkor csökkenti a vércukorszintet a szervezetben, ha az magas.
A Mounjaro-t elhízott vagy túlsúlyos (legalább 27 kg/m2 testtömegindex- (BMI) értékkel rendelkező) felnőttek kezelésére is alkalmazzák. A Mounjaro befolyásolja az étvágyszabályozást, ami segíthet abban, hogy kevesebb ételt egyen, és csökkentse a testtömegét.
A Mounjaro-t 2-es típusú cukorbetegség esetén a következő esetekben alkalmazzák:
- önmagában, ha nem szedhet metformint (egy másik cukorbetegség kezelésére szolgáló gyógyszert);
- egyéb cukorbetegség kezelésére szolgáló gyógyszerrel együtt, ha azokkal a vércukorszintje nem kontrollálható megfelelő mértékben. Ilyen gyógyszer lehet szájon át szedhető készítmény és/vagy inzulin, amelyet injekció formájában kell beadni.
A Mounjaro-t diétával és testmozgással együtt a testtömeg csökkentésére és a testtömeg kontrollálására is alkalmazzák olyan felnőtteknél, akiknek:
- a testtömegindex (BMI) értéke 30 kg/m2 vagy annál nagyobb (elhízás), vagy
- a testtömegindex (BMI) értéke legalább 27 kg/m2, de kevesebb mint 30 kg/m2 (túlsúly), és akik emellett testtömeggel összefüggő egészségügyi problémákkal küzdenek (mint például a cukorbetegséget megelőző állapot (prediabétesz), a 2-es típusú cukorbetegség, a magasvérnyomás-betegség, a kóros vérzsírszint, az alvás alatt jelentkező "obstruktív alvási apnoé szindróma" nevű légzési probléma, illetve a kórelőzményben szereplő szívinfarktus, agyi érkatasztrófa (sztrók) vagy az érbetegség).
A testtömegindex (BMI) az Ön magasságához viszonyított testtömegét mérő szám.
Fontos, hogy továbbra is betartsa a diétára és a testmozgásra vonatkozó tanácsokat, melyeket a kezelőorvosa, a gondozását végző egészségügyi szakember vagy a gyógyszerésze adott.
2. Tudnivalók a Mounjaro KwikPen alkalmazása előtt
Ne alkalmazza a Mounjaro KwikPen-t:
- ha allergiás a tirzepatidra vagy a gyógyszer (6. pontban felsorolt) egyéb összetevőjére.
Figyelmeztetések és óvintézkedések
A Mounjaro alkalmazása előtt beszéljen kezelőorvosával, a gondozását végző egészségügyi szakemberrel vagy gyógyszerészével, ha:
- súlyos emésztési problémái vannak, vagy az étel a szokottnál hosszabb ideig marad a gyomrában (beleértve az úgynevezett súlyos gasztroparézist is).
- korábban volt már hasnyálmirigy-gyulladása (pankreatitisze, ami nem múló, erős hasi fájdalommal és hátfájással járhat).
- szemproblémái vannak (diabéteszes retinopátia vagy makulaödéma).
- szulfonilureát (egy másik diabétesz kezelésére szolgáló gyógyszert) vagy inzulint alkalmaz a cukorbetegsége kezelésére, mivel alacsony vércukorszint (hipoglikémia) alakulhat ki. A kockázat csökkentése érdekében lehet, hogy kezelőorvosának meg kell változtatnia ezen egyéb gyógyszerek adagját.
A Mounjaro-kezelés megkezdésekor bizonyos esetekben folyadékvesztést/kiszáradást tapasztalhat, például hányás, hányinger és/vagy hasmenés miatt, ami a veseműködés csökkenéséhez vezethet.
Fontos, hogy bő folyadékbevitellel megelőzze a kiszáradást. Ha bármilyen kérdése vagy aggálya van, forduljon kezelőorvosához.
Ha tudja, hogy olyan műtét előtt áll, amelyet érzéstelenítéssel (altatással) végeznek, kérjük, tájékoztassa kezelőorvosát, hogy Mounjaro-t alkalmaz.
Gyermekek és serdülők
Ez a gyógyszer nem adható 18 évesnél fiatalabb gyermekeknek és serdülőknek, mivel a gyógyszert ebben a korcsoportban nem vizsgálták.
Egyéb gyógyszerek és a Mounjaro
Feltétlenül tájékoztassa kezelőorvosát, a gondozását végző egészségügyi szakembert vagy gyógyszerészét a jelenleg vagy nemrégiben alkalmazott, valamint alkalmazni tervezett egyéb gyógyszereiről.
Terhesség
Ha Ön terhes, illetve, ha fennáll Önnél a terhesség lehetősége vagy gyermeket szeretne, a gyógyszer alkalmazása előtt beszéljen kezelőorvosával. Ez a gyógyszer nem alkalmazható terhesség alatt, mivel a gyógyszer magzatra gyakorolt hatása nem ismert. Ezért a gyógyszer alkalmazása során fogamzásgátlás alkalmazása javasolt.
Szoptatás
Nem ismert, hogy a tirzepatid kiválasztódik-e az anyatejbe. Az újszülöttre/csecsemőre nézve a kockázatot nem lehet kizárni. Ha Ön szoptat vagy szoptatni szeretne, a gyógyszer alkalmazása előtt beszéljen kezelőorvosával. Önnek és kezelőorvosának kell eldöntenie, hogy abba kell-e hagynia a szoptatást, vagy el kell halasztani a Mounjaro alkalmazását.
A készítmény hatásai a gépjárművezetéshez és a gépek kezeléséhez szükséges képességekre
Nem valószínű, hogy ez a gyógyszer befolyásolja a gépjárművezetéshez és a gépek kezeléséhez szükséges képességeket. Ha azonban a Mounjaro-t szulfonilureával vagy inzulinnal együtt alkalmazza, alacsony vércukorszint (hipoglikémia) jelentkezhet, ami csökkentheti az Ön koncentrálóképességét.
Kerülje a gépjárművezetést vagy a gépek kezelését, ha az alacsony vércukorszint bármilyen jelét tapasztalja, például fejfájás, álmosság, gyengeség, szédülés, éhségérzet, zavartság, ingerlékenység, szapora szívverés és izzadás (lásd 4. pont). Az alacsony vércukorszint fokozott kockázatára vonatkozó információkat lásd a 2. pontban a "Figyelmeztetések és óvintézkedések" részben. További információkért forduljon kezelőorvosához.
A Mounjaro KwikPen nátriumot tartalmaz
A készítmény kevesebb mint 1 mmol (23 mg) nátriumot tartalmaz adagonként, azaz gyakorlatilag "nátriummentes".
A Mounjaro KwikPen benzil-alkoholt tartalmaz
Ez a gyógyszer 5,4 mg benzil-alkoholt tartalmaz 0,6 ml-es adagonként. A benzil-alkohol allergiás reakciókat okozhat.
Ha Ön terhes vagy szoptat, illetve, ha máj- vagy vesebetegségben szenved, kérje ki kezelőorvosa, a gondozását végző egészségügyi szakember vagy gyógyszerésze tanácsát. Erre azért van szükség, mert a nagy mennyiségben alkalmazott benzil-alkohol felhalmozódhat a testében és mellékhatásokat okozhat (úgynevezett metabolikus acidózis).
3. Hogyan kell alkalmazni a Mounjaro KwikPen-t?
A gyógyszert mindig kezelőorvosa vagy gyógyszerésze által elmondottaknak megfelelően alkalmazza. Amennyiben nem biztos abban, hogyan alkalmazza a gyógyszert, kérdezze meg kezelőorvosát vagy gyógyszerészét.
Mennyit kell alkalmaznia
- A gyógyszer kezdő adagja heti egyszer 2,5 mg négy héten át. Négy hét elteltével kezelőorvosa heti egyszeri 5 mg-ra emeli az adagot.
- Ha szükséges, kezelőorvosa 2,5 mg-os lépésekben heti egyszeri 7,5 mg-ra, 10 mg-ra, 12,5 mg-ra vagy 15 mg-ra emelheti az adagot. Kezelőorvosa minden esetben el fogja mondani Önnek, hogy az adott adagot legalább 4 héten át kell alkalmazni, mielőtt nagyobb adagra váltana.
Ne változtassa meg az adagját, kivéve, ha kezelőorvosa utasítást ad rá.
Válassza ki, hogy mikor szeretné alkalmazni a Mounjaro-t
Az injekciós tollat a nap folyamán bármikor, étkezés közben vagy attól függetlenül is alkalmazhatja. Lehetőség szerint minden héten ugyanazon a napon kell alkalmaznia. Emlékeztetőül, hogy mikor kell a Mounjaro-t alkalmaznia, érdemes bejelölni egy naptárban.
Szükség esetén megváltoztathatja a Mounjaro injekció heti beadásának napját, amennyiben az utolsó injekció beadása óta legalább 3 nap eltelt. Az új beadási nap kiválasztása után folytassa a heti egyszeri adagolást az új napon.
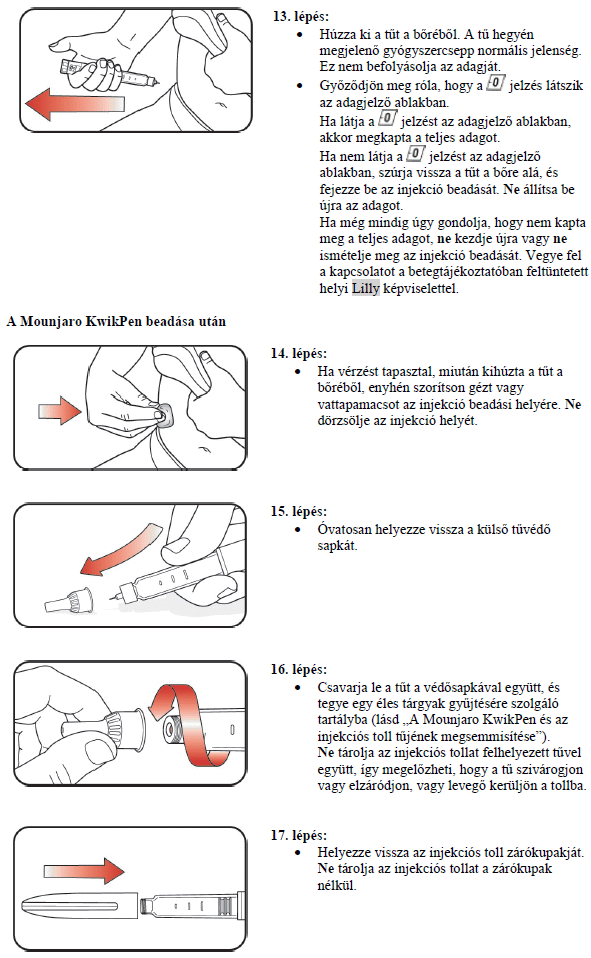
Hogyan kell a Mounjaro KwikPen-t beadni?
A Mounjaro-t a bőr alá (szubkután injekcióként) kell beadni a hasba, a köldöktől legalább 5 cm-re, a combba vagy a felkarba. Amennyiben a felkarba szeretné beadni az injekciót, szüksége lehet más valaki segítségére.
Ha szeretné, adhatja a gyógyszert minden héten ugyanarra a testtájra. Azonban figyeljen arra, hogy az adott testtájon belül mindig változtassa meg az injekció beadási helyét. Amennyiben inzulininjekciót is használ, válasszon másik beadási helyet az injekció beadásához.
A Mounjaro KwikPen alkalmazása előtt kérjük, figyelmesen olvassa el az injekciós tollra vonatkozó "Használati útmutató"-t.
A vércukorszint ellenőrzése
Fontos, hogy a kezelőorvosa, a gondozását végző egészségügyi szakember vagy a gyógyszerésze útmutatása alapján ellenőrizze a vércukorszintjét, ha a Mounjaro-t szulfonilureával vagy inzulinnal együtt alkalmazza (lásd a 2. pontban a "Figyelmeztetések és óvintézkedések" részt).
Ha az előírtnál több Mounjaro-t alkalmazott
Amennyiben a szükségesnél több Mounjaro-t alkalmazott, azonnal forduljon a kezelőorvosához. Ebből a gyógyszerből a túl nagy mennyiség alacsony vércukorszintet (hipoglikémia) és hányingert vagy hányást okozhat.
Ha elfelejtette alkalmazni a Mounjaro-t
Ha elfelejtett beadni egy adagot,
- és 4 nap vagy annál kevesebb telt el azóta, hogy be kellett volna adnia a Mounjaro-t, minél előbb adja be, amint eszébe jut. Ezután a következő adagot a szokásos módon, a tervezett napon adja be.
- Ha több mint 4 nap telt el azóta, hogy be kellett volna adnia a Mounjaro-t, hagyja ki az elfelejtett adagot. Ezután a következő adagot a szokásos módon, a tervezett napon adja be.
Ne alkalmazzon kétszeres adagot a kihagyott adag pótlására. Két adag között legalább 3 napnak kell eltelnie.
Ha idő előtt abbahagyja a Mounjaro alkalmazását
Ne hagyja abba a Mounjaro alkalmazását anélkül, hogy kezelőorvosával ezt megbeszélné. Ha abbahagyja a Mounjaro alkalmazását és Ön 2-es típusú cukorbetegségben szenved, megemelkedhet a vércukorszintje.
Ha bármilyen további kérdése van a gyógyszer alkalmazásával kapcsolatban, kérdezze meg kezelőorvosát, a gondozását végző egészségügyi szakembert vagy gyógyszerészét.
4. Lehetséges mellékhatások
Mint minden gyógyszer, így ez a gyógyszer is okozhat mellékhatásokat, amelyek azonban nem mindenkinél jelentkeznek.
Súlyos mellékhatások
Nem gyakori (100-ból legfeljebb 1 beteget érinthet)
- Hasnyálmirigy-gyulladás (akut pankreatitisz), amely nem múló, erős hasi fájdalmat és hátfájást okozhat. Azonnal forduljon orvoshoz, ha ezeket a tüneteket észleli.
Ritka (1000-ből legfeljebb 1 beteget érinthet)
- Súlyos allergiás reakciók (például anafilaxiás reakció, angioödéma). Azonnali orvosi segítséget kell kérnie, és tájékoztatnia kell kezelőorvosát, ha olyan tüneteket tapasztal, mint a légzési problémák, az ajkak, a nyelv és/vagy a torok gyorsan kialakuló duzzanata nyelési nehézséggel, valamint szapora szívverés.
Egyéb mellékhatások
Nagyon gyakori (10-ből több mint 1 beteget érinthet)
- hányinger;
- hasmenés;
- hasi fájdalom, amiről a testtömeg kontrollálása miatt kezelt betegeknél számoltak be;
- hányás, amiről a testtömeg kontrollálása miatt kezelt betegeknél számoltak be;
- székrekedés, amiről a testtömeg kontrollálása miatt kezelt betegeknél számoltak be.
Ezek a mellékhatások általában nem súlyosak. Hányinger, hasmenés és hányás leggyakrabban akkor fordulnak elő, amikor először kezdik el a tirzepatid-kezelést, de gyakoriságuk a legtöbb betegnél idővel csökken.
- Az alacsony vércukorszint (hipoglikémia) nagyon gyakori, ha a tirzepatidot szulfonilureával és/vagy inzulinnal együtt alkalmazzák. Ha szulfonilureát vagy inzulint alkalmaz a 2-es típusú cukorbetegség kezelésére, lehet, hogy ezek adagját csökkenteni kell a tirzepatid alkalmazásakor (lásd a 2. pontban a "Figyelmeztetések és óvintézkedések" részt). Az alacsony vércukorszint tünetei közé tartozhat a fejfájás, álmosság, gyengeség, szédülés, éhségérzet, zavartság, ingerlékenység, gyors szívverés és az izzadás. Kezelőorvosa elmagyarázza Önnek, hogy hogyan kell kezelni az alacsony vércukorszintet.
Gyakori (10-ből legfeljebb 1 beteget érinthet)
- alacsony vércukorszint (hipoglikémia), ha a tirzepatidot metforminnal, illetve nátrium-glükóz kotranszporter-2-gátlóval (a cukorbetegség kezelésére szolgáló másik gyógyszerrel) együtt alkalmazzák a 2-es típusú cukorbetegség kezelésére;
- allergiás reakció (túlérzékenység) (például bőrkiütés, viszketés és ekcéma);
- szédülés, amiről a testtömeg kontrollálása miatt kezelt betegeknél számoltak be;
- alacsony vérnyomás, amiről a testtömeg kontrollálása miatt kezelt betegeknél számoltak be;
- az éhségérzet csökkenése (étvágycsökkenés), amiről a 2-es típusú cukorbetegség miatt kezelt betegeknél számoltak be;
- hasi fájdalom, amiről a 2-es típusú cukorbetegség miatt kezelt betegeknél számoltak be;
- hányás, amiről a 2-es típusú cukorbetegség miatt kezelt betegeknél számoltak be - általában idővel csökken;
- emésztési zavar (diszpepszia);
- székrekedés, amiről a 2-es típusú cukorbetegség miatt kezelt betegeknél számoltak be;
- haspuffadás;
- böfögés (eruktáció);
- bélgázképződés (flatulencia);
- reflux vagy gyomorégés (gasztroözofageális refluxbetegségnek (GERD) is nevezik) - ez egy olyan kórkép, amit a gyomorból a nyelőcsőbe (a gyomrot és a szájat összekötő csőbe) visszaáramló sav okoz;
- hajhullás, amiről a testtömeg kontrollálása miatt kezelt betegeknél számoltak be;
- fáradtságérzés;
- az injekció beadási helyén kialakuló reakciók (például viszketés vagy bőrpír);
- gyors pulzus;
- a hasnyálmirigyenzimek (például lipáz és amiláz) vérszintjének növekedése;
- emelkedett kalcitoninszint a vérben a testtömeg kontrollálása miatt kezelt betegeknél.
Nem gyakori (100-ból legfeljebb 1 beteget érinthet)
- alacsony vércukorszint (hipoglikémia), ha a tirzepatidot metforminnal együtt alkalmazzák a 2-es típusú cukorbetegség kezelésére;
- epekövesség;
- az epehólyag gyulladása;
- fogyás, amiről a 2-es típusú cukorbetegség miatt kezelt betegeknél számoltak be;
- az injekció beadási helyén fellépő fájdalom;
- emelkedett kalcitoninszint a vérben a 2-es típusú cukorbetegség miatt kezelt betegeknél;
- az ízérzés megváltozása.
Mellékhatások bejelentése
Ha Önnél bármilyen mellékhatás jelentkezik, tájékoztassa erről kezelőorvosát, a gondozását végző egészségügyi szakembert vagy gyógyszerészét. Ez a betegtájékoztatóban fel nem sorolt bármilyen lehetséges mellékhatásra is vonatkozik. A mellékhatásokat közvetlenül a hatóság részére is bejelentheti az alábbi elérhetőségek valamelyikén keresztül:
Nemzeti Népegészségügyi és Gyógyszerészeti Központ, Postafiók 450, H-1372 Budapest
honlap: https://ogyei.gov.hu
elektronikus bejelentő form: https://mellekhatas.ogyei.gov.hu/
e-mail: adr.box@nngyk.gov.hu
A mellékhatások bejelentésével Ön is hozzájárulhat ahhoz, hogy minél több információ álljon rendelkezésre a gyógyszer biztonságos alkalmazásával kapcsolatban.
5. Hogyan kell a Mounjaro KwikPen-t tárolni?
A gyógyszer gyermekektől elzárva tartandó!
Az injekciós toll címkéjén és a dobozon feltüntetett lejárati idő (EXP) után ne alkalmazza ezt a gyógyszert. A lejárati idő az adott hónap utolsó napjára vonatkozik.
Hűtőszekrényben (2 °C-8 °C) tárolandó. Nem fagyasztható! Ha az injekciós toll megfagyott, NE HASZNÁLJA!
A Mounjaro KwikPen az első használat után hűtés nélkül legfeljebb 30 °C-on, legfeljebb 30 napig tárolható, majd ezután az injekciós tollat meg kell semmisíteni.
Ne alkalmazza ezt a gyógyszert, ha az injekciós toll megsérült, vagy a gyógyszer zavaros, elszíneződött vagy részecskéket lát benne.
Semmilyen gyógyszert ne dobjon a szennyvízbe vagy a háztartási hulladékba. Kérdezze meg gyógyszerészét, hogy mit tegyen a már nem használt gyógyszereivel. Ezek az intézkedések elősegítik a környezet védelmét.
6. A csomagolás tartalma és egyéb információk
Mit tartalmaz a Mounjaro KwikPen?
A készítmény hatóanyaga a tirzepatid.
Mounjaro 2,5 mg/adag KwikPen: 2,5 mg tirzepatidot tartalmaz 0,6 ml oldatban, adagonként. 10 mg tirzepatidot tartalmaz 2,4 ml oldatban (4,17 mg/ml), többadagos előretöltött injekciós tollanként. Minden injekciós toll 4, egyenként 2,5 mg-os adagot tartalmaz.
Mounjaro 5 mg/adag KwikPen: 5 mg tirzepatidot tartalmaz 0,6 ml oldatban, adagonként. 20 mg tirzepatidot tartalmaz 2,4 ml oldatban (8,33 mg/ml), többadagos előretöltött injekciós tollanként. Minden injekciós toll 4, egyenként 5 mg-os adagot tartalmaz.
Mounjaro 7,5 mg/adag KwikPen: 7,5 mg tirzepatidot tartalmaz 0,6 ml oldatban, adagonként. 30 mg tirzepatidot tartalmaz 2,4 ml oldatban (12,5 mg/ml), többadagos előretöltött injekciós tollanként. Minden injekciós toll 4, egyenként 7,5 mg-os adagot tartalmaz.
Mounjaro 10 mg/adag KwikPen: 10 mg tirzepatidot tartalmaz 0,6 ml oldatban, adagonként. 40 mg tirzepatidot tartalmaz 2,4 ml oldatban (16,7 mg/ml), többadagos előretöltött injekciós tollanként. Minden injekciós toll 4, egyenként 10 mg-os adagot tartalmaz.
Mounjaro 12,5 mg/adag KwikPen: 12,5 mg tirzepatidot tartalmaz 0,6 ml oldatban, adagonként. 50 mg tirzepatidot tartalmaz 2,4 ml oldatban (20,8 mg/ml), többadagos előretöltött injekciós tollanként. Minden injekciós toll 4, egyenként 12,5 mg-os adagot tartalmaz.
Mounjaro 15 mg/adag KwikPen: 15 mg tirzepatidot tartalmaz 0,6 ml oldatban, adagonként. 60 mg tirzepatidot tartalmaz 2,4 ml oldatban (25 mg/ml), többadagos előretöltött injekciós tollanként. Minden injekciós toll 4, egyenként 15 mg-os adagot tartalmaz.
Egyéb összetevők: dinátrium-hidrogén-foszfát-heptahidrát (E339), benzil-alkohol (E1519) (további információkért lásd a 2. pontban "A Mounjaro KwikPen benzil-alkoholt tartalmaz" részt), glicerin, fenol, nátrium-klorid, nátrium-hidroxid (további információkért lásd a 2. pontban "A Mounjaro nátriumot tartalmaz" részt), tömény sósav és injekcióhoz való víz.
Milyen a Mounjaro külleme és mit tartalmaz a csomagolás?
A Mounjaro tiszta, színtelen vagy halványsárga színű oldatos injekció előretöltött injekciós tollban (KwikPen).
2,4 ml (4 adag 0,6 ml-es) oldatos injekciót, valamint a légtelenítéshez szükséges többletmenyiséget tartalmazza előretöltött KwikPen-enként. A csomagolás nem tartalmaz tűket.
1 db vagy 3 db KwikPen-t tartalmazó csomagolás.
Nem feltétlenül mindegyik kiszerelés kerül kereskedelmi forgalomba.
Használati útmutató
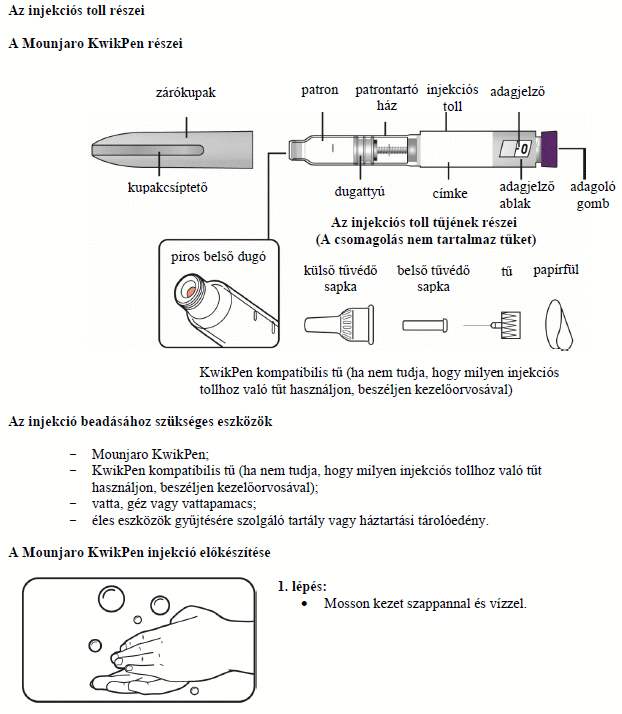
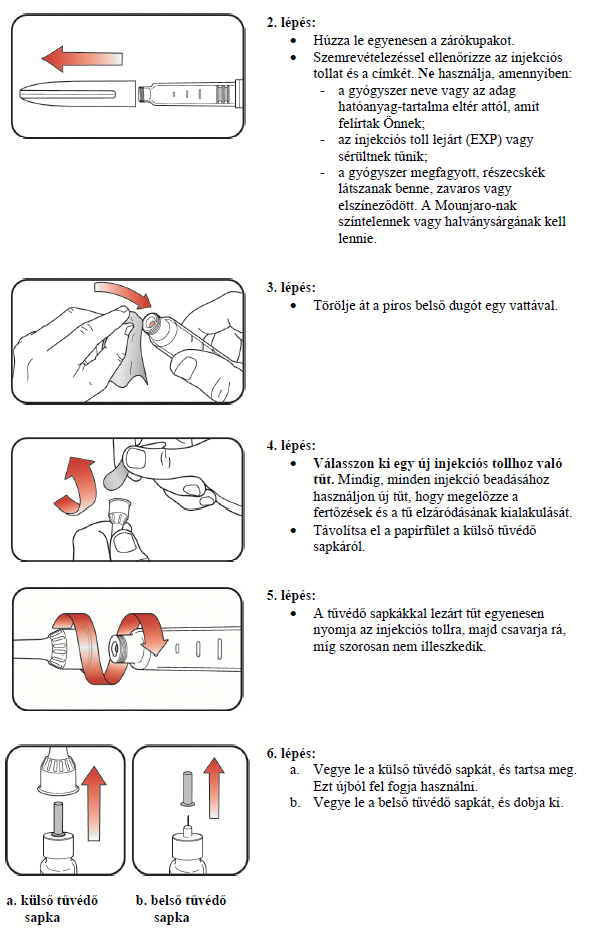
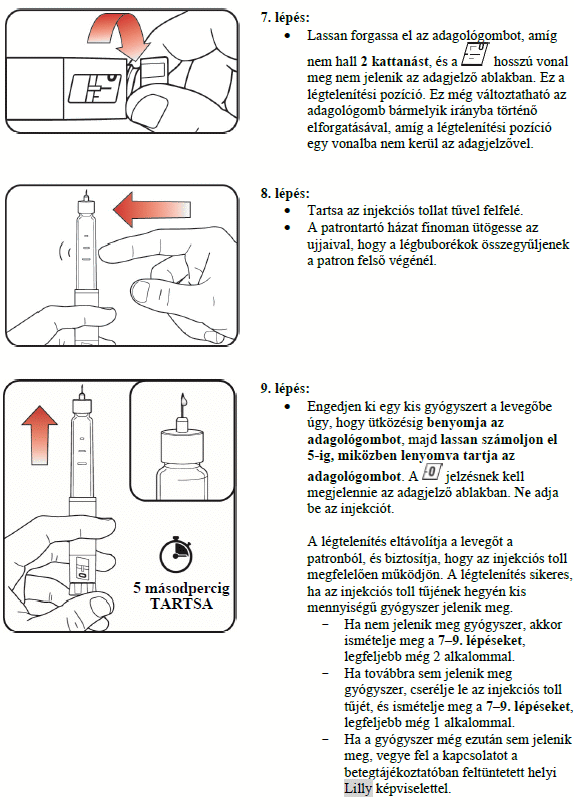
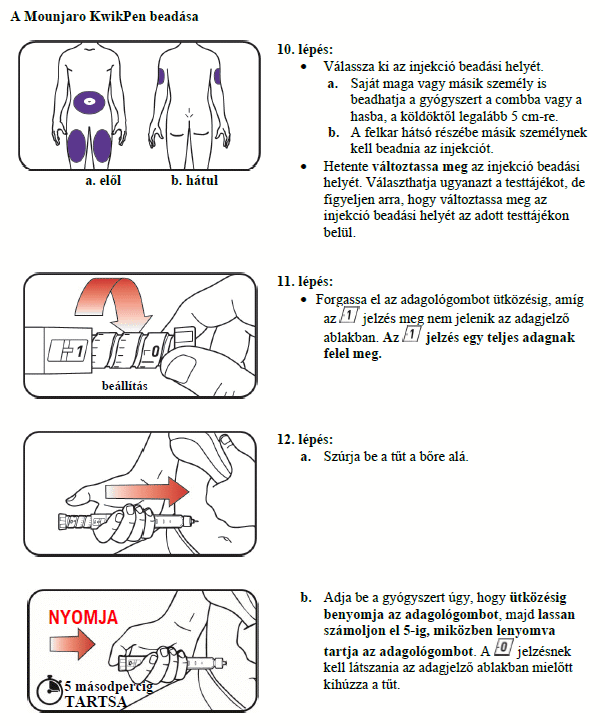
A Mounjaro KwikPen tárolása
Nem használt injekciós toll:
- A még nem használt injekciós tollakat hűtőszekrényben, 2 °C és 8 °C között tárolja.
- A még nem használt injekciós tollak a címkén található lejárati időn belül felhasználhatóak, amennyiben azokat hűtőszekrényben tárolták.
- Ne fagyassza le az injekciós tollat! Semmisítse meg az injekciós tollat, ha az korábban megfagyott.
Használt injekciós toll:
- A használt injekciós tollat legfeljebb 30 °C-os szobahőmérsékleten tárolhatja.
- Az injekciós toll és a tűk gyermekektől elzárva tartandók!
- Az első használat után 30 nappal semmisítse meg az injekciós tollat, még akkor is, ha az injekciós tollban maradt gyógyszer.
- A 4 heti adag beadása után semmisítse meg az injekciós tollat. Ha megpróbálja beadni a maradék gyógyszert, az nem teljes dózis beadásához vezethet, még akkor is, ha az injekciós tollban maradt még gyógyszer.
A Mounjaro KwikPen és az injekciós toll tűjének megsemmisítése
- Tegye az injekciós toll használt tűit egy éles tárgyak gyűjtésére szolgáló tartályba vagy egy zárt fedelű, kemény műanyag tartályba.
- Ne dobja az injekciós tollról levett tűket a háztartási hulladékba.
- A használt injekciós tollat a kezelőorvosa utasításának megfelelően semmisítse meg.
- Kérdezze meg kezelőorvosától, hogy milyen lehetőségei vannak az éles tárgyak gyűjtésére szolgáló tartály megfelelő megsemmisítésére.
- Ne használja újra az éles tárgyak gyűjtésére szolgáló tartályt.
Gyakori kérdések
- Ha nem tudja eltávolítani a zárókupakot, finoman tekerje előre-hátra, majd egyenesen húzza le.
- Ha nehéz benyomni az adagológombot:
-- ha lassabban nyomja meg az adagológombot, könnyebb lesz az injekció beadása.
-- elzáródhatott a tű. Helyezzen fel egy új tűt, és légtelenítse az injekciós tollat.
-- por, étel vagy folyadék lehet az injekciós tollban. Semmisítse meg az injekciós tollat, és használjon egy újat.
További információk
Ha bármilyen kérdése vagy problémája van a Mounjaro KwikPen-nel kapcsolatban:
- Vegye fel a kapcsolatot a Lilly helyi képviseletével, kezelőorvosával, a gondozását végző egészségügyi szakemberrel vagy gyógyszerészével.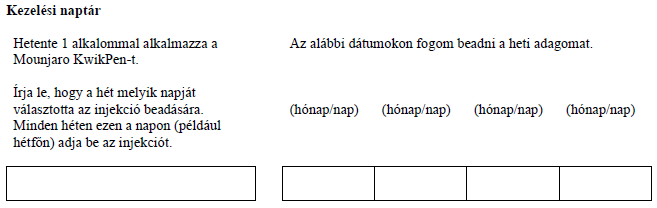
A szöveg publikálásának dátuma az ema.europa.eu weboldalon: 2024.10.25.
