ALPROLIX 250 NE por és oldószer oldatos injekcióhoz
Hatóanyag:
eftrenonacog alfa
Csak vényre kapható
Kiszerelés:
1x porüveg+oldószerüveg

Tájékoztató ár:
-
Normatív TB-támogatás:
Nem
Eü. emelt támogatás:
Nem
-
Gyógyszerfőkategória:
K-VITAMIN ÉS EGYÉB VÉRZÉSCSILLAPÍTÓ SZEREK
-
Törzskönyvi szám:
EU/1/16/1098/001
-
Gyógyszeralkategória:
Véralvadási faktorok
-
Gyártó:
Swedish Orphan Biovitrum AB
Betegtájékoztató
1. Milyen típusú gyógyszer az ALPROLIX és milyen betegségek esetén alkalmazható?
Az ALPROLIX az eftrenonakog-alfa nevű hatóanyagot tartalmazza, amely egy rekombináns technológiával előállított IX-es alvadási faktor, Fc fúziós fehérje. A IX-es faktor a szervezetben természetes módon termelődő fehérje, amely szükséges ahhoz, hogy a vér megalvadjon, és a vérzés elálljon.
Az ALPROLIX vérzések kezelésére és megelőzésére alkalmazható a B-típusú vérzékenységben (hemofília B, a IX-es faktor hiánya által előidézett örökletes vérzészavar) szenvedő betegek valamennyi korcsoportjában.
Az ALPROLIX-ot rekombináns technológiával állítják elő anélkül, hogy a gyártási folyamat során bármilyen emberi vagy állati eredetű összetevőt adnának hozzá.
Hogyan hat az ALPROLIX?
Hemofília B-ben szenvedő betegeknél a IX-es faktor hiányzik vagy nem működik megfelelően. Ezt a gyógyszert a hiányzó vagy hibás IX-es faktor pótlására alkalmazzák. Az ALPROLIX emeli a vérben a IX-es faktor szintjét, és átmenetileg korrigálja a vérzéshajlamot. A gyógyszerben található Fc fúziós fehérje növeli a gyógyszer hatásának időtartamát.
2. Tudnivalók az ALPROLIX alkalmazása előtt
Ne alkalmazza az ALPROLIX-ot
- ha allergiás az eftrenonakog-alfára vagy a gyógyszer (6. pontban felsorolt) egyéb összetevőjére.
Figyelmeztetések és óvintézkedések
Az ALPROLIX alkalmazása előtt beszéljen kezelőorvosával, gyógyszerészével vagy a gondozását végző egészségügyi szakemberrel.
- Van rá egy kis esély, hogy az ALPROLIX anafilaxiás reakciót (hirtelen kezdődő, súlyos allergiás reakciót) váltson ki Önnél. Az allergiás reakciók tünetei közé tartozhat a testszerte jelentkező viszketés, csalánkiütés, mellkasi feszülés, nehézlégzés és alacsony vérnyomás. Amennyiben ezen tünetek bármelyike jelentkezik, azonnal szakítsa meg az injekció beadását, és forduljon kezelőorvosához. Az allergiás reakciók IX-es faktor alkalmazásakor fennálló kockázata miatt az ALPROLIX első beadását orvosi megfigyelés alatt kell végezni, ahol az allergiás reakciók megfelelő ellátása biztosítható.
- Ha úgy véli, hogy nem uralható a vérzése az Önnek rendelt adaggal, beszéljen kezelőorvosával, mivel ennek számos oka lehet. Például a hemofília B kezelése során előforduló ismert szövődmény az ellenanyagok (más néven gátlótestek) kialakulása. Az ellenanyagok megakadályozzák, hogy a kezelés megfelelően kifejtse hatását. Ezt kezelőorvosa ellenőrizni fogja. Ne emelje meg a vérzés csillapítása céljából alkalmazott ALPROLIX teljes adagját anélkül, hogy kezelőorvosával megbeszélte volna.
IX-es faktor inhibitorral (gátlótesttel) rendelkező betegnél fokozott lehet az anafilaxia kockázata a IX-es faktorral végzett későbbi kezelés során. Ezért, amennyiben Ön a fent említett allergiás reakciókat tapasztalja, ki kell Önt vizsgálni inhibitorok jelenlétére.
A IX-es faktor készítmények fokozhatják a nemkívánatos vérrögök kockázatát a szervezetben, különösen, ha vérrögképződés kockázati tényezői állnak fenn Önnél. A lehetséges nemkívánatos vérrögképződés tünetei közé tartozhat: fájdalom és/vagy érzékenység egy visszér mentén, a kar vagy a láb váratlan megdagadása vagy hirtelen kialakuló légszomj, illetve légzési nehézség.
Szív- és érrendszeri események
Ha azt mondták Önnek, hogy szívbetegsége van, vagy fennáll Önnél a szívbetegség kockázata, fokozott elővigyázatossággal alkalmazza a IX-es faktort, és beszéljen kezelőorvosával.
Katéterrel kapcsolatos szövődmények
Amennyiben Önnél centrális vénás katéter alkalmazása szükséges, mérlegelni kell a centrális vénás katéterrel kapcsolatos szövődmények, köztük a helyi fertőzés, baktériumok vérben való jelenléte és a katéter helyén kialakuló vérrögök kockázatát.
Dokumentálás
Hangsúlyozottan ajánlott, hogy az ALPROLIX beadásakor minden alkalommal feljegyezze a készítmény nevét és a gyártási tétel számát.
Egyéb gyógyszerek és az ALPROLIX
Feltétlenül tájékoztassa kezelőorvosát vagy gyógyszerészét a jelenleg vagy nemrégiben szedett, valamint szedni tervezett egyéb gyógyszereiről.
Terhesség és szoptatás
Ha Ön terhes vagy szoptat, illetve ha fennáll Önnél a terhesség lehetősége vagy gyermeket szeretne, a gyógyszer alkalmazása előtt beszéljen kezelőorvosával vagy gyógyszerészével.
A készítmény hatásai a gépjárművezetéshez és a gépek kezeléséhez szükséges képességekre
Az ALPROLIX nem befolyásolja a gépjárművezetéshez és a gépek kezeléséhez szükséges képességeket.
Az ALPROLIX nátriumot tartalmaz.
A gyógyszer kevesebb mint 1 mmol (23 mg) nátriumot tartalmaz injekciós üvegenként, azaz gyakorlatilag "nátriummentes". Ha a kezeléshez egynél több injekciós üvegre van szükség, figyelembe kell venni a teljes nátriumtartalmat.
3. Hogyan kell alkalmazni az ALPROLIX-ot?
Az ALPROLIX-szal végzett kezelést olyan orvos fogja megkezdeni, aki jártas a hemofíliában szenvedő betegek ellátásában. A gyógyszert mindig a kezelőorvosa által elmondottaknak megfelelően alkalmazza (lásd 7. pont). Amennyiben nem biztos az adagolást illetően, kérdezze meg kezelőorvosát, gyógyszerészét vagy a gondozását végző egészségügyi szakembert.
Az ALPROLIX-ot injekció formájában, vénába kell beadni. A készítményt megfelelő oktatás után Ön vagy valaki más is beadhatja Önnek. Kezelőorvosa fogja kiszámítani (nemzetközi egységben (NE) kifejezve), az adagot, ami az Ön IX-es faktorpótló terápia iránti egyéni igényétől, valamint attól függ, hogy vérzés megelőzésére vagy kezelésére alkalmazza-e a készítményt. Ha úgy véli, hogy nem uralható a vérzése az Önnek rendelt adaggal, beszéljen kezelőorvosával.
Az, hogy milyen gyakran szükséges injekciót kapnia attól függ, hogy mennyire hatásos Önnél ez a gyógyszer. Kezelőorvosa megfelelő laborvizsgálatokat fog végeztetni, hogy meggyőződjön róla, megfelelő-e a vérében a IX-es faktor szintje.
Vérzés kezelése
Az ALPROLIX adagját az Ön testtömege és az elérni kívánt IX-es faktorszinttől függően kell kiszámolni.
A IX-es faktorszint célértéke a vérzés súlyosságától és elhelyezkedésétől függ.
Vérzés megelőzése
Ha az ALPROLIX-ot vérzés megelőzésére alkalmazza, kezelőorvosa fogja kiszámítani Önnek az adagot.
Az ALPROLIX szokásos adagja 50 NE testtömeg-kilogrammonként hetente egyszer adva, vagy 100 NE testtömeg-kilogrammonként, 10 naponta adva. Kezelőorvosa módosíthatja az adagot vagy az adagolás gyakoriságát. Egyes esetekben, különösen fiatalabb betegek kezelésekor, rövidebb adagolási időszakok vagy nagyobb adagok lehetnek szükségesek.
Alkalmazása gyermekeknél és serdülőknél
Az ALPROLIX a gyermekek és serdülők valamennyi korcsoportjában alkalmazható. 12 év alatti gyermekeknél nagyobb adagokra vagy az injekciók gyakoribb adására lehet szükség, a szokásos adag 50-60 NE testtömeg kilogrammonként, 7 naponta adva.
Ha az előírtnál több ALPROLIX-ot alkalmazott
Tájékoztassa kezelőorvosát, amint lehetséges. Az ALPROLIX-ot mindig a kezelőorvosa által elmondottaknak megfelelően alkalmazza. Amennyiben nem biztos az adagolást illetően, kérdezze meg kezelőorvosát, gyógyszerészét vagy a gondozását végző egészségügyi szakembert.
Ha elfelejtette alkalmazni az ALPROLIX-ot
Ne alkalmazzon kétszeres adagot a kihagyott adag pótlására. Adja be a szokásos adagot, amint eszébe jut, majd folytassa a szokásos adagolási rend szerint. Ha a teendőket illetően kétségei lennének, forduljon kezelőorvosához, gyógyszerészéhez vagy a gondozását végző egészségügyi szakemberhez.
Ha idő előtt abbahagyja az ALPROLIX alkalmazását
Ne hagyja abba az ALPROLIX alkalmazását anélkül, hogy kezelőorvosával megbeszélte volna. Ha abbahagyja az ALPROLIX alkalmazását, a továbbiakban nem feltétlenül lesz védett a vérzéssel szemben, illetve lehetséges, hogy az aktuálisan fennálló vérzés nem szűnik meg.
Ha bármilyen további kérdése van a gyógyszer alkalmazásával kapcsolatban, kérdezze meg kezelőorvosát, gyógyszerészét vagy a gondozását végző egészségügyi szakembert.
4. Lehetséges mellékhatások
Mint minden gyógyszer, így ez a gyógyszer is okozhat mellékhatásokat, amelyek azonban nem mindenkinél jelentkeznek.
Ha súlyos, hirtelen kezdetkialakuló allergiás reakciók (anafilaxiás reakció) lépnek fel, az injekció beadását azonnal le kell állítani. Azonnal kezelőorvosához kell fordulnia, ha az allergiás reakciók következő tüneteinek bármelyikét tapasztalja: arcduzzanat, kiütés, testszerte jelentkező viszketés, csalánkiütés, mellkasi feszülés, nehézlégzés, égő és csípő érzés az injekció beadásának helyén, hidegrázás, kipirulás, fejfájás, általános rosszullét, hányinger, nyugtalanság, gyors szívverés és alacsony vérnyomás.
IX-es faktorra ható gyógyszerekkel korábban nem kezelt gyermekeknél gyakran (10 beteg közül legfeljebb 1 betegnél) képződhetnek gátlószerek (lásd 2. pont). Ha ez bekövetkezik, lehetséges, hogy a gyógyszer nem működik tovább megfelelően és gyermeke tartós vérzést tapasztalhat. Ilyen esetben azonnal forduljon kezelőorvosához.
A gyógyszer alkalmazásakor a következő mellékhatások jelentkezhetnek:
Gyakori mellékhatások (10 beteg közül legfeljebb 1 beteget érinthet): fejfájás, szájzsibbadás vagy bizsergés, oldalsó deréktáji fájdalom, amelyet véres vizelet kísér (obstruktív uropátia) és bőrpír az injekció helyén.
IX-es faktorra ható gyógyszerekkel korábban nem kezelt gyermekek: IX-es faktor-gátlók, túlérzékenység.
Nem gyakori mellékhatások (100 beteg közül legfeljebb 1 beteget érinthet): szédülés, az ízérzés megváltozása, rossz lehelet, fáradtságérzés, az injekció beadásának helyén jelentkező fájdalom, gyors szívverés, vér megjelenése a vizeletben (hematúria), oldalsó deréktáji fájdalom (vesekólika), alacsony vérnyomás és csökkent étvágy.
Mellékhatások bejelentése
Ha Önnél bármilyen mellékhatás jelentkezik, tájékoztassa kezelőorvosát, gyógyszerészét vagy a gondozását végző egészségügyi szakembert. Ez a betegtájékoztatóban fel nem sorolt bármilyen lehetséges mellékhatásra is vonatkozik. A mellékhatásokat közvetlenül a hatóság részére is bejelentheti az alábbi elérhetőségek valamelyikén keresztül: Országos Gyógyszerészeti és Élelmezés-egészségügyi Intézet, Postafiók 450, H-1372 Budapest, Magyarország, honlap: www.ogyei.gov.hu. A mellékhatások bejelentésével Ön is hozzájárulhat ahhoz, hogy minél több információ álljon rendelkezésre a gyógyszer biztonságos alkalmazásával kapcsolatban.
5. Hogyan kell az ALPROLIX-ot tárolni?
A gyógyszer gyermekektől elzárva tartandó!
A dobozon és az injekciós üveg címkéjén feltüntetett lejárati idő "EXP" után ne alkalmazza ezt a gyógyszert. A lejárati idő az adott hónap utolsó napjára vonatkozik. Ne alkalmazza ezt a gyógyszert, ha 6 hónapnál hosszabb ideig volt szobahőmérsékleten tárolva.
Hűtőszekrényben (2 °C-8 °C) tárolandó. Nem fagyasztható! A fénytől való védelem érdekében az eredeti csomagolásban tárolandó.
Másik lehetőségként az ALPROLIX tárolható szobahőmérsékleten (legfeljebb 30 °C-on), 6 hónapot meg nem haladó egyszeri időtartamban. Az ALPROLIX hűtőszekrényből való kivételének és szobahőmérsékletre helyezésének dátumát jegyezze fel a dobozra. Szobahőmérsékleten történt tárolás után a készítményt tilos visszatenni a hűtőszekrénybe.
Az ALPROLIX-ot elkészítése után azonnal fel kell használni. Ha azonnal nem tudja felhasználni az elkészített oldatot, akkor szobahőmérsékleten történő tárolás esetén 6 órán belül kell felhasználni. Az oldat elkészítése után hűtőszekrényben nem tárolható! Az oldat közvetlen napfénytől védve tartandó.
Az elkészített oldat tiszta vagy enyhén opálos és színtelen lesz. Ne alkalmazza ezt a gyógyszert, ha zavaros vagy látható részecskéket tartalmaz.
A készítmény kizárólag egyszeri használatra szolgál.
A fel nem használt oldatot megfelelő módon ki kell dobni. Semmilyen gyógyszert ne dobjon a szennyvízbe vagy a háztartási hulladékba. Kérdezze meg gyógyszerészét, hogy mit tegyen a már nem használt gyógyszereivel. Ezek az intézkedések elősegítik a környezet védelmét.
6. A csomagolás tartalma és egyéb információk
Mit tartalmaz az ALPROLIX?
Por:
- A készítmény hatóanyaga az eftrenonakog-alfa (rekombináns IX-es alvadási faktor, Fc fúziós fehérje). Az ALPROLIX névlegesen 250, 500, 1000, 2000 vagy 3000 NE eftrenonakog-alfát tartalmaz injekciós üvegenként.
- Egyéb összetevők a szacharóz, hisztidin, mannit, poliszorbát 20, nátrium-hidroxid és sósav. Amennyiben Ön csökkentett nátriumtartalmú étrendet tart, lásd a 2. pontot.
Oldószer:
5 ml nátrium-klorid és injekcióhoz való víz.
Milyen az ALPROLIX külleme és mit tartalmaz a csomagolás?
Az ALPROLIX oldatos injekcióhoz való por és oldószer formájában kerül forgalomba. A por fehér vagy törtfehér por vagy pogácsa. Az oldat elkészítéséhez biztosított oldószer tiszta, színtelen oldat. Elkészítése után az oldat tiszta vagy enyhén opálos és színtelen.
Az ALPROLIX minden csomagja a következőket tartalmazza: 1 db port tartalmazó injekciós üveget, 5 ml oldószert előretöltött fecskendőben, 1 db dugattyúrudat, 1 db injekciósüveg-adaptert, 1 db infúziós szereléket, 2 db alkoholos törlőt, 2 db ragtapaszt, 1 db gézlapot.
7. Az elkészítésre és beadásra vonatkozó utasítások
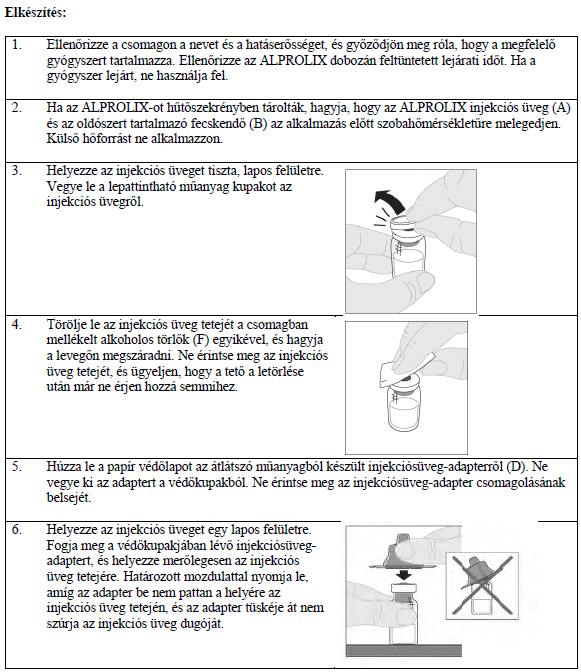

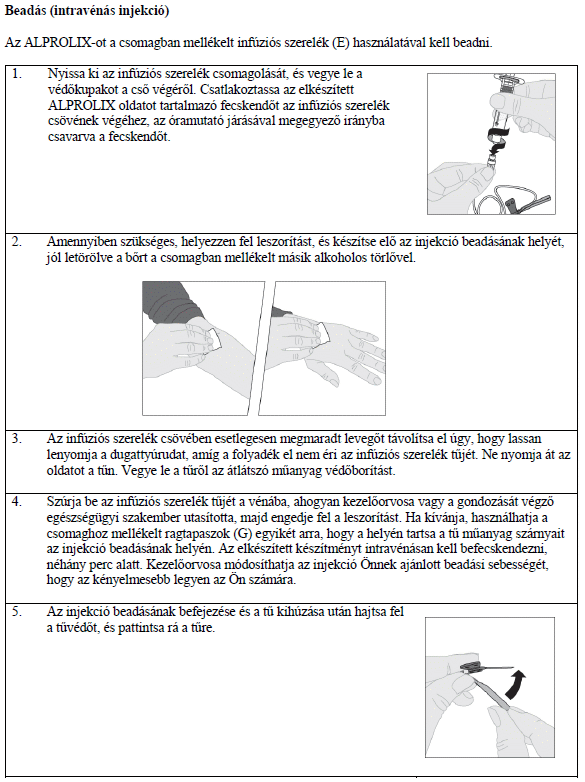

A szöveg publikálásának dátuma az ema.europa.eu weboldalon: 2021.03.17.
